Comprende l'articulation pathologique
En anatomie, le terme «articulation» fait référence à toutes les manières de relier deux parties du squelette entre elles. L'articulation du genou ou celle de la hanche, est le type d'articulation le plus complexe, aux capacités fonctionnelles hautement développées. Cependant quel que soit leur type, nos articulations partagent entre elles une série de structures comparables: os sous-chondral, cartilage, synovie, qui sont disposées de manière variable en fonction de la contrainte mécanique à assurer.
L'articulation saine
Le cartilage
Le cartilage est un tissu conjonctif spécialisé, de consistance dure, mais non minéralisé, contrairement au tissu osseux. En condition physiologique, ce tissu n’est ni innervé, ni vascularisé. Cependant, le cartilage lésé lors d’une pathologie peut présenter des zones de vascularisation. Un seul type cellulaire, le chondrocyte, est présent au sein d’une matrice extracellulaire (MEC) abondante et complexe. Les chondrocytes sont en partie responsables de la synthèse ainsi que de la dégradation de cette matrice. Chez l'Homme adulte, on distingue trois types de cartilage (Mallein-Gerin F. et Van der Rest M., 1996) selon la composition de la matrice extracellulaire : le cartilage fibreux, ou fibrocartilage, qui constitue par exemple les disques intervertébraux, le cartilage élastique, que l’on retrouve par exemple au niveau des oreilles, et le cartilage hyalin, qui recouvre les surfaces articulaires.
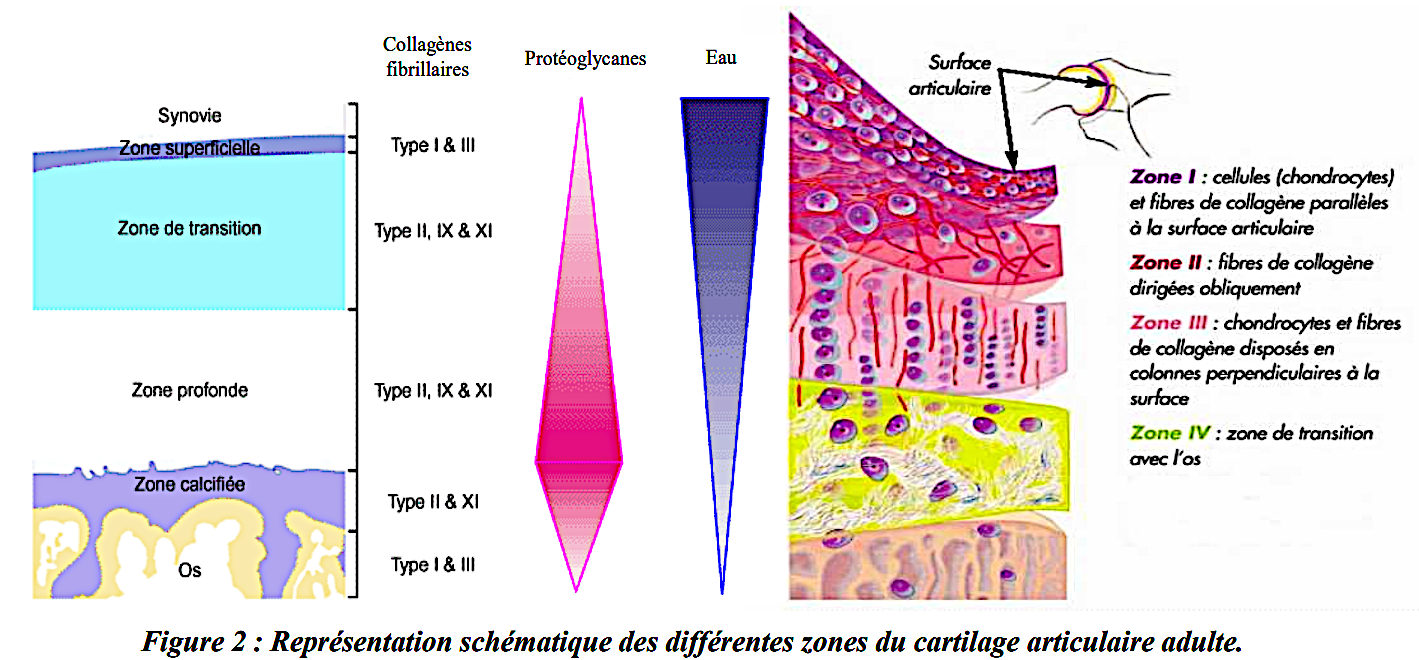
- la zone superficielle, ou tangentielle, très fine. Elle est en contact avec le liquide synovial, et sert donc de surface de « glissement », tout en étant la zone la plus exposée aux contraintes mécaniques. Cette couche représente environ 5 à 10 % de la hauteur totale du cartilage.
- la zone intermédiaire ou de transition : elle constitue la deuxième couche du cartilage, formée de fibres de collagène de type II, IX et XI qui s'entrecroisent obliquement en un réseau non orienté, moins dense que celui de la zone superficielle.
- la zone radiale ou profonde : elle contient également des fibres de collagène de type II, IX et XI, mais celles-ci sont orientées de façon perpendiculaire à la surface du cartilage. Les chondrocytes de cette zone sont présents en faible densité, arrondis et moins volumineux
- la zone calcifiée : elle est en contact avec la plaque osseuse sous-chondrale à laquelle elle ancre le cartilage et représente entre 5 et 10 % de l'épaisseur totale du cartilage (Figure 2). Elle correspond à une zone où le cartilage est en voie de calcification.
Composition du cartilage
La matrice extra cellulaire
La MEC est principalement constituée d’eau (65 à 80 %), de collagènes (10 à 30 % du poids humide du cartilage), de PGs (5 à 10 % du poids humide du cartilage), de hyaluronate, et, en quantité moins importante, de protéines non-collagéniques et de lipides.
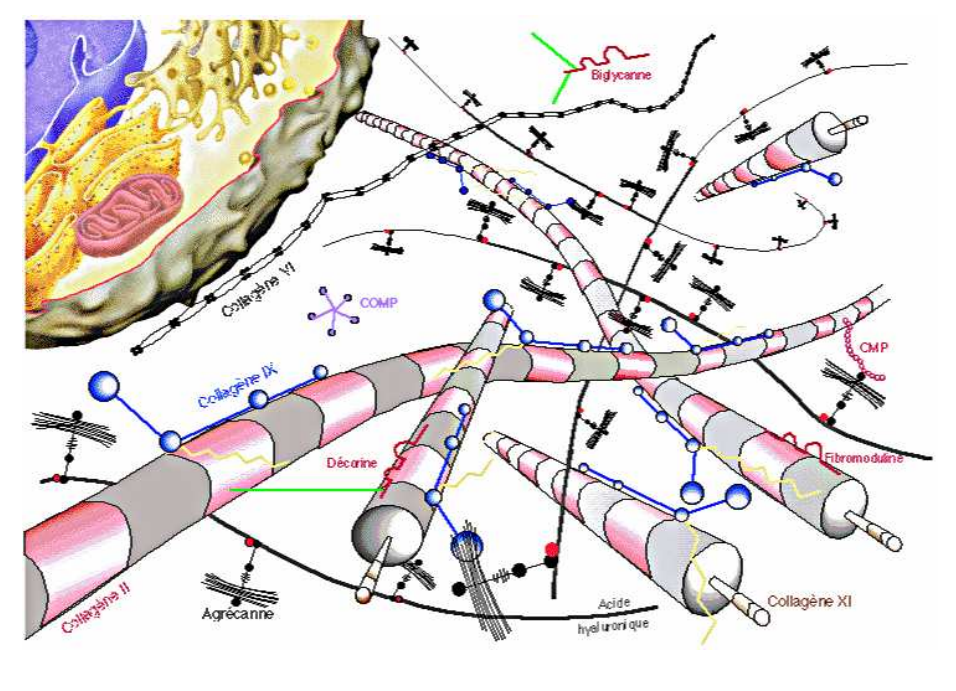
Les collagènes
Le collagène de type II :
Collagène le plus représenté au sein du cartilage mature (Corvol M.T., 1996). Il forme un réseau dense dont les mailles emprisonnent les agrégats de PGs, ce qui limite l’entrée d’eau dans le tissu. C’est le principal responsable de la résistance aux forces de traction et de compression, ainsi que du maintien de la forme et de la structure tissulaire.
Le collagène de type VI:
Stabilise et interagit avec les molécules de hyaluronate pour favoriser les relations cellule/matrice. Le collagène de type IX:
Stabilise et favorise la croissance latérale des fibres de collagène de type II.
Le collagène de type X :
Est retrouvé en petites quantités dans le cartilage adulte normal. Il est principalement localisé dans les zones hypertrophiques du cartilage, et les sites de fracture.
Le collagène de type XI:
polymérise avec le collagène de type II, et interagit avec l’héparane et l’héparine sulfate pour réguler le diamètre des fibres de collagène II.
Les protéoglycanes (PGs)
Les PGs contribuent à la répartition des contraintes mécaniques sur une surface maximale de l’os sous-chondral.
Ils sont classés en deux catégories selon leur poids moléculaire :
. Les PGs de haut poids moléculaire, formant de larges agrégats, comme par exemple, l’agrécane. Celui-ci représente environ 90 % des PGs. Ces PGs, du fait de leur fort poids moléculaire, jouent un rôle majeur dans les propriétés biomécaniques du cartilage (amortissement des chocs notamment).
. Les PGs de faible poids moléculaire, tels la décorine, le byglicane, ou la fibromoduline, représentent environ 3 % du tissu cartilagineux.
Les chondrocytes
Le chondrocyte tire son nom du grec : chondros (χουδρο), qui signifie « cartilage » et kytos (χντος), qui signifie « cellule ». Littéralement, le chondrocyte est donc la « cellule du cartilage ». Ces cellules sont de forme sphérique et elles sont volumineuses(5 à 10 % du volume du tissu dans le cartilage articulaire adulte humain).
Ces cellules présentent deux stades de prolifération :
1) lors de la phase de croissance du cartilage (chez l’enfant), les cellules sont actives et prolifèrent en mode axial (ligne droite) ou coronaire (cercle) ;
2) à l’âge adulte, les cellules cessent de proliférer, puis le nombre de chondrocytes diminue avec l’âge. Les cellules passent alors du stade de cellule active, volumineuse, au stade de cellule de réserve et enfin au stade de dégénérescence ou de nécrose.
Les chondrocytes supportent deux types de contraintes :
. La pression dynamique (mise en charge, marche), perpendiculaire à la surface, qui augmente l’activité cellulaire.
. La pression statique, qui, elle, diminue l’activité métabolique cellulaire.
L’activité métabolique du chondrocyte est donc fortement liée aux contraintes mécaniques imposées. Lors d’une pathologie dégénérative du cartilage comme l’arthrose, le cartilage etdégradé, la matrice péricellulaire tend alors à augmenter. La cellule perçoit alors moins bien les signaux mécaniques et les réponses métaboliques sont donc anormales.
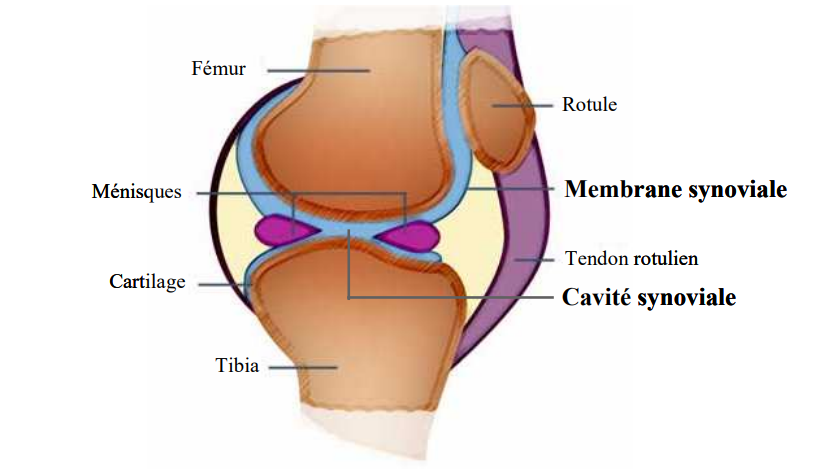
La membrane synoviale
La membrane synoviale est un tissu conjonctif lâche hautement spécialisé qui tapisse l’intérieur de l’articulation. Elle sécrète le liquide synovial qui lubrifie l’articulation grâce à son coefficient de friction très bas, et nourrit le cartilage grâce à la présence de nombreux vaisseaux sanguins. Elle est divisée en deux couches:
- Une couche qui délimite la cavité articulaire,
- une couche de revêtement qui tapisse la capsule articulaire.
La membrane synoviale est composée en majorité de fibres élastiques et de tissu adipeux. Elle est richement vascularisée et innervée, ce qui participe au phénomène douloureux dans un contexte de maladie articulaire de nature inflammatoire ou dégénérative
Elle possède trois types de fonctions : tout d’abord une fonction mécanique, de par la sécrétion du liquide synovial, une fonction de nutrition du cartilage, et enfin une fonction de défense contre les infections et l’inflammation. En effet, lors d’une agression mécanique, infectieuse ou inflammatoire, la membrane synoviale s’épaissit, sécrète en excès du liquide synovial, ce qui crée un épanchement. Elle régule également la pression partielle en oxygène, grâce à sa nature fortement vascularisée.
Dans une articulation saine, le liquide synovial est présent en très faible quantité : il forme un film qui tapisse le cartilage. C’est un liquide transparent ou jaune pâle, limpide, de très forte viscosité. Il est composé principalement d’eau, de sels minéraux, de protéines, d’électrolytes (chlorure, sodium, potassium) et d’urée. Il est riche en hyaluronates (mélange d’acide hyaluronique, de protéines, de polysaccharides, de N-acétylglucosamine et d’acide glucuronique), qui lui confèrent ses propriétés de viscosité. Les hyaluronates forment une sorte de « tamis » qui ne laisse passer que les petites protéines, ce qui explique pourquoi le liquide synovial est dépourvu de fibrinogène, d’immunoglobulines et de macroglobulines. Il est dépourvu de cellule en absence de pathologie.
L'articulation pathologique
Les pathologies articulaires sont caractérisées par une modification et une altération progressives de la structure de la membrane synoviale et du cartilage, et même des structures environnantes comme l’os ou les tendons (Figure 5). Ceci entraîne, avec le temps, une perte de la fonction articulaire.
Les types de pathologies
Il existe cent types de pathologies articulaires différentes, dont les deux formes les plus communes sont:
- Les arthropathies dites dégénératives, comme l’arthrose, pour lesquellesla destruction du cartilage est un phénomène clé.
- Les arthropathies inflammatoires, telle que la polyarthrite rhumatoïde(PR), pour laquelle la destruction du cartilage n’est qu’un facteur secondaire par rapport à l’inflammation initiée dans la synoviale.
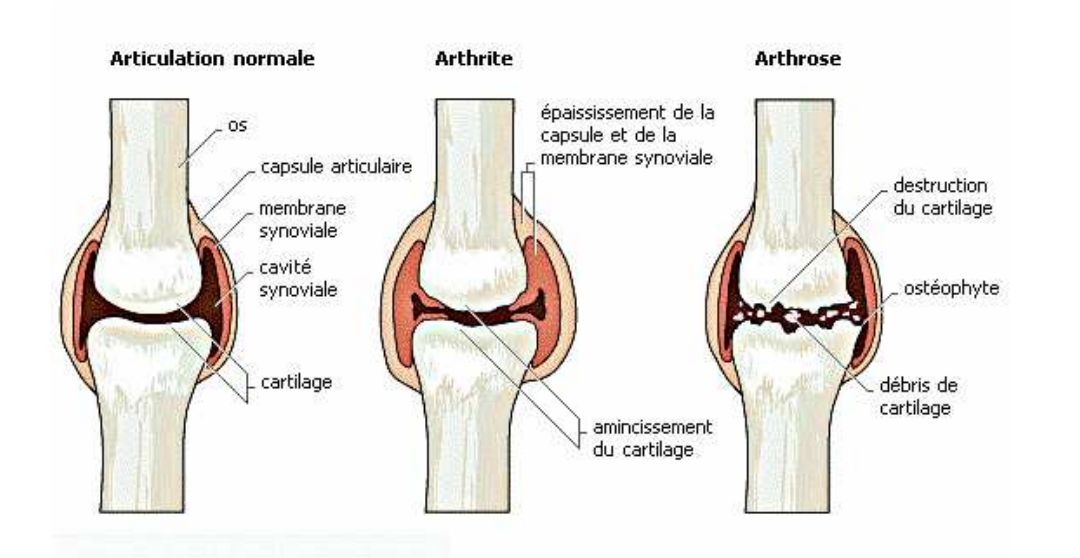
Au cours d’une pathologie articulaire, toutes les structures de l’articulation sont atteintes : le cartilage, la synoviale, l’os et même les tendons. Lors du développement de l’arthrite, la synoviale s’hypertrophie et le cartilage s’amincit. Au cours de l’arthrose, le cartilage est dégradé et l’os sous-chondral est mis à nu.
L'arthose
maladie dégénérative, multifactorielle, qui induit des modifications morphologiques, biochimiques, moléculaires, et biomécaniques du cartilage, qui entraînent la perte d’homéostasie du cartilage. Elle n’est pas considérée comme une arthropathie inflammatoire car peu de neutrophiles sont présents dans le liquide synovial et il n’y a pas de manifestation inflammatoire systémique. L’arthrose aboutit à une chondromalacie (« ramollissement »), un œdème, une fissuration, une ulcération, et une perte du cartilage, ainsi qu’à une sclérose de l’os sous-chondral. Dans les phases les plus avancées de la maladie, le cartilage disparaît et l’os est mis à nu. La perte du cartilage s’explique par le fait que les chondrocytes adultes sont incapables physiologiquement de combler le déficit en cartilage acquis au cours de la vie. La capacité d’amortissement du cartilage est alors dépassée. À la surface du chondrocyte, le nombre de récepteurs diminue, ce qui restreint sa sensibilité, et induit l’arrêt de la croissance du cartilage.
Des fragments de PG générés par les enzymes des chondrocytes pénètrent dans la cavité synoviale. Cette dernière réagit en sécrétant des collagénase, de la stromélysine et des cytokines qui vont créer un inflammation douloureuse ainsi que la sécrétion de médiateurs inflammatoires dans le liquide synovial
Au cours de la maladie arthrosique, la synoviale est le siège d’une réaction inflammatoire modérée, comparée à celle très importante observée dans la PR. La siginification de cette inflammation reste controversée, et les hypothèses conduisant à la synovite sont diverses : des débris liés à l’usure du cartilage, des cristaux ou des cytokines pro-inflammatoires pourraient causer cette inflammation. Cette réaction intervient tardivement dans l’évolution de la maladie et représente un facteur aggravant. Trois aspects de la synoviale sont possibles au cours de l’arthrose : une synoviale normale, une synoviale réactionnelle (le nombre de villosités augmente et la synoviale devient opaque), ou une synoviale inflammatoire (hypervascularisation, prolifération des villosités, hypertrophie). Fréquemment, ces trois types de synoviales s’observent en différents endroits d’une même articulation. La réaction synoviale est modérée et l’hypertrophie des cellules synoviales bordantes est peu importante. Cependant, la synoviale est le siège d’une réaction fibrosante et d’une inflammation cellulaire non négligeable.
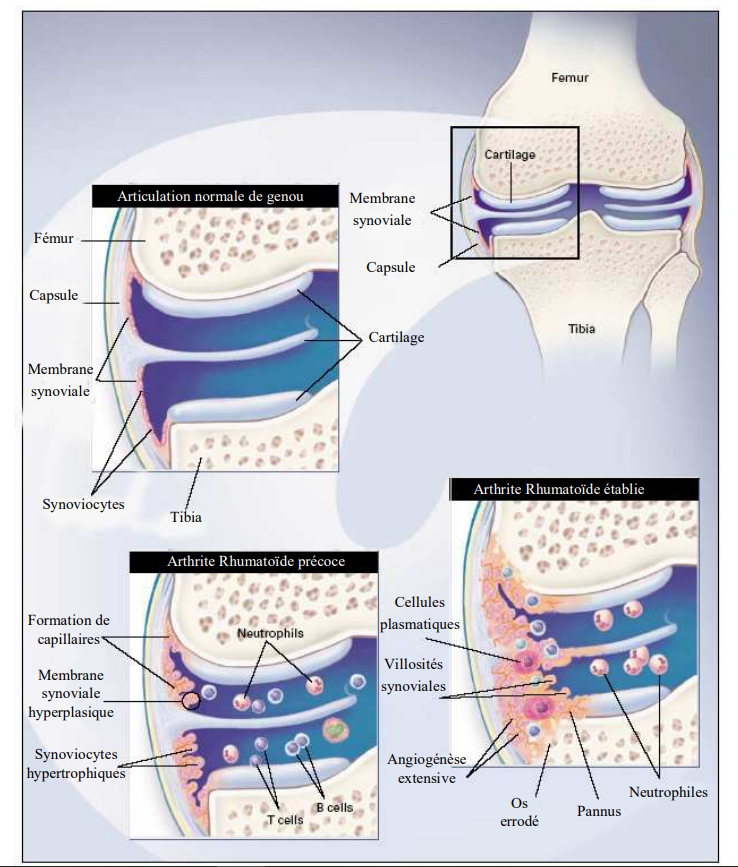
L'arthrite
La polyarthrite rhumatoïde (PR) est un rhumatisme. On appelle rhumatisme toutes les maladies qui touchent à l’appareil locomoteur. Lorsque plusieurs articulations sont touchées, on parle de « polyarthrite ». La PR touche de nombreuses articulations, avec une prédilection pour la main, le poignet, le genou et le pied. Elle est caractérisée par une inflammation chronique de la membrane synoviale, un dysfonctionnement immunitaire et une érosion progressive du cartilage et de l’os.
Contrairement à la pathologie arthrosique, pour laquelle le cartilage est la première structure touchée, la pathologie arthritique touche en premier lieu la synoviale. Celle-ci devient inflammatoire (étiologie méconnue) et produit de fortes quantités de médiateurs inflammatoires, qui vont agir sur le cartilage et engendrer à terme sa destruction. Comme pour l’arthrose, la production en masse de ces médiateurs induit un déséquilibre dans la balance des facteurs pro/anti-inflammatoires qui va conduire à la perte des PGs du cartilage et à l’affaiblissement du réseau collagénique.
Pour ce qui est de la synoviale, l’évolution de la PR peut être décrite en cinq étapes :
- La première étape est cliniquement « silencieuse », elle implique une anomalie de présentation d’un antigène à des lymphocytes T.
- La deuxième étape est déjà symptomatique sur le plan clinique. Elle fait intervenir la prolifération des lymphocytes T et B qui sont associés au phénomène d’angiogenèse de la membrane synoviale.
- La troisième étape est caractérisée par l’activation des synoviocytes résidents, puis des neutrophiles ayant migré dans le liquide synovial. Le cartilage est encore intact à cette étape.
- La quatrième étape est déterminée par l’atteinte de la synoviale qui conduit à l’activation des chondrocytes, puis à la dégradation du cartilage.
- La cinquième et dernière étape est définie par la poursuite de la dégradation du cartilage, entraînant l’érosion de l’os sous-chondral, la prolifération des chondrocytes et l’altération des ligaments.
L’inflammation de la membrane synoviale, ou synovite, est responsable de la douleur et du gonflement articulaire. L’épaississement synovial est quant à lui responsable des lésions ostéocartilagineuses et tendineuses des structures avoisinantes. La membrane synoviale secrète abondamment du liquide synovial, qui s’accumule dans l’articulation pour créer un épanchement. Les cellules de la membrane synoviale se multiplient anormalement et les cellules circulantes s’infiltrent, ce qui conduit à l’épaississement et à la désorganisation de cette membrane.
Les conséquences de toutes ces manifestations sont une destruction progressive du cartilage, de l’os, une érosion, un pincement des articulations, une synovite chronique, une infiltration de lymphocytes entre les surfaces articulaires et le pannus synovial.
Source:
"Étude des effets anti-cytokines et anti-cataboliques des
rétinoïdes sur les fibroblastes synoviaux et les chondrocytes de
rat ou humains stimulés par de l’IL-1β"
- Mélanie KIRCHMEYER
Université de Nancy

0 Commentaires